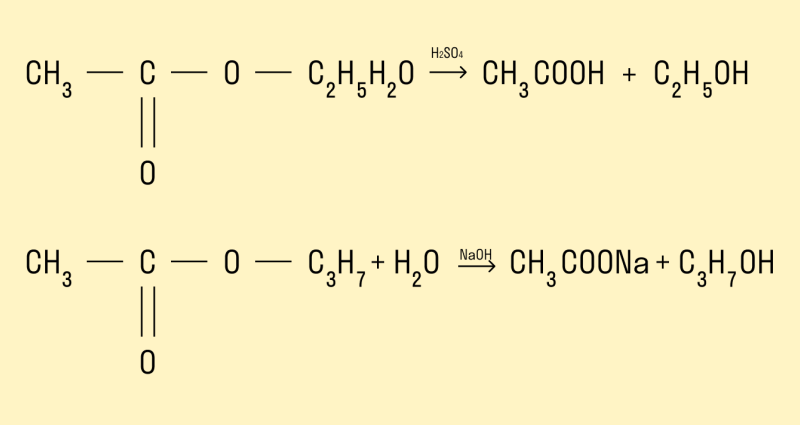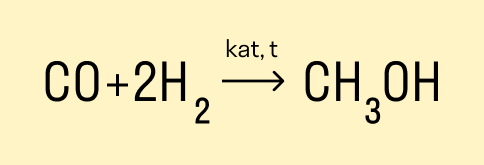Где применяется изопропиловый спирт и можно ли его пить?
Содержание
- 1 Спецификация
- 2 Краткое описание
- 3 Влияние на человека
- 4 Номенклатура спиртов
- 5 Примечания и ссылки
- 6 Возможные последствия
- 7 Получение спиртов
- 8 Какие последствия интоксикации?
- 9 Физические свойства изопропанола
- 10 Почему для стерилизации используют 70% спирт, а не 100?
- 11 Изопропиловый спирт – применение в быту, где продается и чем опасен
- 12 Механизм интоксикации
- 13 Чем изопропанол вреден для здоровья человека?
- 14 Изопропиловый спирт
- 15 Как можно отравиться
- 16 Производство
- 17 Общее описание
- 18 Реакции
Изопропиловый спирт представляет собой прозрачную, бесцветную жидкость с выраженным ароматом. Это летучее, легковоспламеняющееся и многофункциональное химическое соединение. Он используется во многих промышленных и бытовых продуктах и является эффективным антисептическим, противогрибковым и дезинфицирующим средством. Изопропиловый спирт известен под рядом других названий, таких как изопропанол, протирочный спирт и пропан-2-ол. Он является важным ингредиентом многих продуктов, включая чистящие, дезинфицирующие и лекарственные средства. Поскольку изопропиловый спирт является мощным и эффективным антисептиком, его можно использовать для обработки порезов, царапин и небольших ожогов. Изопропиловый спирт также используется в некоторых лабораторных и промышленных условиях, например, при производстве промышленных растворителей и чистящих средств, подробнее на https://nersplus.ru/catalog/izopropilovyy_spirt/. В этой статье блога мы расскажем о различных областях применения изопропилового спирта, его химических свойствах и мерах предосторожности, которые следует соблюдать при работе с ним.
Спецификация
| Массовая доля изопропилового спирта, %, не менее | 99,7 | 87,0 |
| Цветность по платиново-кобальтовой шкале, не более | 5 | 10 |
| Массовая доля кислот в пересчете на уксусную кислоту, % не более | 0,0007 | 0,001 |
| Массовая доля сернистых соединений в пересчете на серу, % не более | 0,00005 | 0,0001 |
| Бромное число, г брома на 100 г спирта, не более | 0,006 | не опеделяется |
| Массовая доля воды, % не более | 0,15 | не опеделяется |
| Массовая доля карбонильных соединений в пересчете на группу СО, %, не более | не опеделяется | 0,8 |
| Массовая доля диизопропилового эфира, % не более | 0,03 | 0,03 |
| Массовая доля ацетона, % не более | 0,03 | 0,03 |
| Массовая доля нелетучего остатка, % не более | 0,0005 | 0,0005 |
Краткое описание
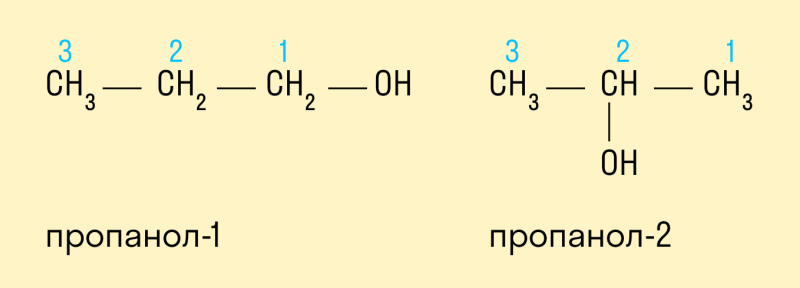
В сфере народного хозяйства большой спрос получил изопропиловый спирт (общая формула — CH3CH (OH)CH3 или C3H8OH). Это органическое соединение было получено в результате проведения лабораторных опытов над пропанолом. Оба вещества относятся к категории простейших спиртов алифатического ряда, из-за чего их свойства имеют много совпадений. В Википедии указано, что CH3CH (OH)CH3 имеет сразу несколько названий:
- пропанол-2 (структурная формула — C3H8O) либо втор-пропанол. Этот элемент получил своё название из-за присоединения гидроксильной группы ко второму углероду молекулы пропана (С3Н8);
- изопропилэтаноат;
- изопропен, изопропилен;
- изобутиловый, изопентиловый спирт;
- диизопропил;
- изопропилпентан;
- изопропанол — эта жидкость по принципу строения является изомером обычного пропанола.
- изопропилпропионат;
- диметилкарбинол.
Изопропиловый спирт, или C3H8OH, — это прозрачное, бесцветное органическое соединение, которое широко используется во многих областях повседневной жизни. Эта легковоспламеняющаяся жидкость состоит из атомов водорода и углерода и быстро сгорает, выделяя углекислый газ и воду без дыма и копоти. Поскольку он считается менее токсичным, чем метанол, изопропен становится все более популярным в косметологии. Многие лекарственные препараты местного действия содержат это вещество, и его также можно найти под разными названиями в других повседневных продуктах. В этой статье блога мы подробно рассмотрим применение и преимущества изопропилового спирта, а также возможные риски, связанные с его использованием.
CH3CH (OH)CH3 помогает растворить эфирные масла, смолы, а также другие химические соединения. Изопропиловый спирт хорошо смешивается с Н2О. Благодаря химической реакции это вещество может быть преобразовано в ацетон. Если человек употребит изопропилпентан, то он опьянеет. Но токсичное воздействие будет выше, чем у этанола. Реакция организма на химическое вещество зависит от индивидуальных показателей и объёма выпитой жидкости. Изопропанол отличается низким показателем плотности. При температуре +80 °C органическое соединение закипает. Если попробовать нагреть жидкость до +450 °C, то в итоге она самовоспламенится.
Изопропилпентан активно используют в качестве надёжного консерванта органических веществ и для хранения медицинских анализов. Для этих целей можно задействовать формальдегид, но он является более опасным. Изопропанол часто используют для исследования ДНК. Молекула дезоксирибонуклеиновой кислоты не растворяется в этом спирте. В лабораторных условиях изопропен добавляется в заранее подготовленную ДНК, для того чтобы выполнить преципитирование.
Влияние на человека
- Ингаляционное
Предельно допустимая концентрация (ПДК) паров изопропанола в воздухе рабочей зоны составляет 10 мг/м³ (ГОСТ 9805-84), в атмосферном воздухе населенных мест 0.6 мг/м³(ГН 2.1.6.1338-03). Не накапливается в организме, то есть кумулятивными свойствами не обладает. Необходимо отметить, что изопропиловый спирт значительно менее летуч, чем, например, этанол, и для достижения больших концентраций его паров необходима значительно большая площадь разлива и испарения. Благодаря этому свойству, изопропиловый спирт заменил этиловый в парфюмерии, дезинфицирующих составах, стеклоомывателях и незамерзающих жидкостях.
Изопропанол горюч. При горении даёт яркое пышное пламя, полностью разлагается на простые составляющие — воду и углекислый газ, не вызывая раздражений и иных побочных эффектов. Горение изопропанола не выделяет вредных веществ, копоти и пр.
Испарение изопропанола из емкости с площадью менее 20 см² в помещении более 30 м³ при температуре 30 °C и ниже не вызывает негативных реакций.
- Пероральное
Отравления изопропанолом случайны и в основном происходят с детьми младше 6 лет. Летальный исход от отравления изопропанолом происходит крайне редко.
Небольшие дозы изопропанола, как правило, не вызывают значительных расстройств. Серьёзное токсическое воздействие на здорового взрослого человека при пероральном употреблении может быть достигнуто при дозах порядка 50 мл и более. Изопропанол при приеме внутрь метаболизируется в печени под действием алкогольдегидрогеназы в ацетон, что обусловливает его токсическое действие.
При приеме внутрь вызывает опьянение, сходное с алкогольным. Хотя токсичность изопропанола примерно в 3,5 раза выше, чем у этанола, его опьяняющее действие также выше, но уже в 10 раз. По этой причине смертельные отравления изопропанолом, в сравнении с отравлениями от этилового спирта, случаются реже, так как человек впадает в алкогольный транс гораздо раньше, чем сможет самостоятельно принять смертельную дозу изопропанола (если только не выпил единовременно от 500 мл).
Биологический полураспад изопропилового спирта в организме человека составляет от 2,5 до 8 часов.
Наркотические свойства
Изопропиловый спирт обладает наркотическим действием. Наркотический эффект изопропанола почти в 2 раза превышает аналогичный эффект этанола. Концентрация 12 промилле в организме человека, воздействующая в течение 4 часов вызывает состояние наркоза и смерть.
При длительном воздействии больших концентраций паров вызывает головную боль, оказывает раздражающее воздействие на глаза и дыхательные пути. Для достижения данного эффекта потребуется находиться в течение длительного времени в непроветриваемом помещении с большой площадью разлива изопропанола. Может оказывать угнетающее действие на центральную нервную систему. Воздействие на уровне, значительно превышающем ПДК, может вызвать потерю сознания. Отравление изопропиловым спиртом возникает нечасто.
| Общие | |
|---|---|
| Систематическоенаименование | Пропанол-2 |
| Традиционные названия | Изопропиловый спирт |
| Хим. формула | C3H8O |
| Рац. формула | CH3CH(OH)CH3 |
| Физические свойства | |
| Состояние | жидкость |
| Молярная масса | 60,09 г/моль |
| Плотность | 0,7851 г/см³ |
| Динамическая вязкость | 0,00243 Па·с |
| Энергия ионизации | 10,1±0,1 эВ |
| Термические свойства | |
| Т. плав. | -89,5 °C |
| Т. кип. | 82,4 °C |
| Т. всп. | 11,7 °C |
| Т. свспл. | 400 °C |
| Пр. взрв. | 2±1 об.% |
| Мол. теплоёмк. | 155,2 Дж/(моль·К) |
| Давление пара | 4,4 кПа при 20 °C |
| Химические свойства | |
| pKa | 16,5 |
| Растворимость в бензоле | хорошо растворим |
| Растворимость в ацетоне | растворим |
| Оптические свойства | |
| Показатель преломления | 1,3776 |
Используется для денатурации этилового спирта, получения пероксида водорода, ацетона, изопропиламина, изопропилацетата, метилизобутилкетона. Также употребляется в промышленности, в токарных и фрезерных работах, при резании алюминия. Изопропиловый спирт входит в состав бытовой химии, косметики, дезинфицирующих средств, репеллентов, средств для автомобилей, к примеру, в состав антифриза, тормозной жидкости, используется в качестве растворителя для зимних стеклоомывателей, входит в состав промывок для печатных плат после пайки с флюсом.
Номенклатура спиртов
По систематической номенклатуре ИЮПАК (IUPAC)
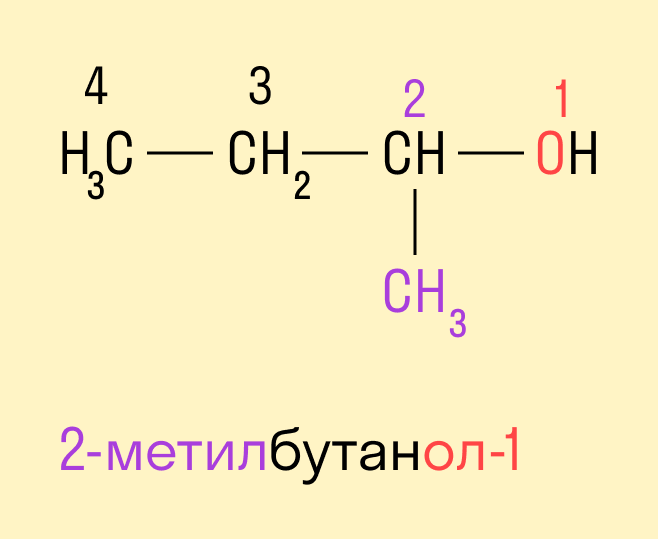
Спиртам дают название по названию углеводорода с добавлением суффикса -ол и цифры, которая показывает положение гидроксильной группы. Для того, чтобы правильно определить, с каким по счету атомом углерода соединена гидроксильная группа, необходимо учитывать следующие правила:
- Выбрать самую длинную углеводородную цепь, в состав которой входит гидроксильная группа. Таким образом устанавливают число атомов углерода и соответственно формируют название.
- Нумерацию длинной цепи осуществляют с того края, к которому ближе расположена гидроксильная группа.
- Местоположение гидроксогруппы в названии определяют написанием цифры после суффикса -ол.
Если в составе спирта присутствуют другие функциональные группы, то нумерация углеродного скелета начинается с того края, где расположена старшая функциональная группа. В таком случае перед названием указывают цифрой, от какого атома углерода идет ответвление.
Радикально-функциональная номенклатура
По такому способу название спирта формируется от названия радикала с добавлением слова «спирт». Например:
- СH3—OH — метанол или метиловый спирт;
- C2H5OH — этанол или этиловый спирт;
- CH3—CH2—CH2—СН2—OH — бутанол или бутиловый спирт.
Примечания и ссылки
- ↑ и
- ↑ and
- рассчитывается молекулярная масса от .
- (in) Ицхак Маркус, Свойства растворителей, т. 4, Англия, John Wiley & Sons Ltd,1999 г., 239 с. ( ISBN 0-471-98369-1 )
- ↑ и (ru) Роберт Х. Перри и Дональд В. Грин, Perry’s Chemical Engineers ‘Handbook, США, McGraw-Hill,1997 г., 7- е изд. , 2400 с. ( ISBN 0-07-049841-5 ), стр. 2-50
- Справочник Ланге по химии, 10-е изд. стр. 1669–1674
- (in) Клаудио А. Фаундес и Хосе О. Вальдеррама, « Модели коэффициента активности для описания парожидкостного равновесия в тройных водно-спиртовых растворах », Китайский журнал химической инженерии, Vol. 17, п о 2апрель 2009 г., стр. 259-267 ( DOI )
- (in) Карл Л. Яс, Справочник по термодинамическим диаграммам: неорганические соединения и элементы, Vol. 1, Хьюстон, Техас, паб Gulf. Co.,1996 г., 384 с. ( ISBN 0-88415-857-8 )
- (in) Дэвид Р. Лид, Справочник по химии и физике, Бока-Ратон, CRC,2008 г., 89- е изд. , 2736 с. ( ISBN 978-1-4200-6679-1 ), стр. 10-205
- , по состоянию на 18 февраля 2009 г.
- ↑ и (in) на , по состоянию на 23 августа 2009 г.
- «Правило спиртов C-201.1». Номенклатура органической химии («Синяя книга» ИЮПАК), разделы A, B, C, D, E, F и H. Oxford: Pergamon Press. 1979. «Такие обозначения, как изопропанол, втор-бутанол и трет-бутанол, неверны, потому что не существует углеводородов изопропана, втор-бутана и трет-бутана, к которым можно было бы добавить суффикс« -ол »; от таких названий следует отказаться . Изопропиловый спирт, втор-бутиловый спирт и трет-бутиловый спирт, однако, допустимы (см. Правило C-201.3), поскольку радикалы изопропил, втор-бутил и трет-бутил действительно существуют ».
- Perron-Roach D (1998) Удовлетворяет ли институциональный подход потребностям своей клиентуры? Справочные материалы: Обзор социальных и общественных вмешательств в Онтарио, 4 (2), 106-114.
Возможные последствия
Даже если человеку вовремя оказали помощь и провели все необходимые лечебные мероприятия, то нельзя полностью исключить отдаленные последствия интоксикации. Отравление может крайне отрицательно сказаться на состоянии внутренних органов и спровоцировать возникновение следующих патологий:
- гастрита и язвенных процессов желудка;
- токсического нефроза почек;
- цирроза печени;
- расстройств функции желез внутренней секреции;
- остаточных неврологических нарушений (периодических головных болей, расстройств координации движений, паралича);
- бронхита и астмы (при отравлении парами).
Все это говорит о том, что изопропиловый спирт категорически нельзя употреблять внутрь. Это может привести не только к опасной интоксикации, но и к инвалидности на фоне тяжелых осложнений.
Изопропиловый спирт — это простейший вторичный спирт, который получают путем прямой и сернокислотной гидрации пропилена.
Изопропиловый спирт имеет 2 разновидности:
- Изопропиловый спирт технический;
- Спирт изопропиловый абсолютированный.
По своим свойствам и составу абсолютированный спирт можно отнести к техническим спиртам. Абсолютированный спирт является наиболее распространенным и востребованным, поскольку в отличие от этилового спирта, его оборот не контролируется на законодательном уровне. Сегодня абсолютированный спирт активно используется в различных промышленных отраслях.
Получение спиртов
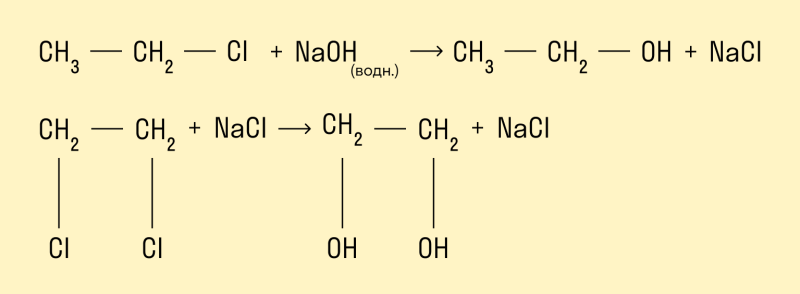
Гидролиз галогенопроизводных алканов
Галогенпроизводные алканов реагируют с водным раствором щелочей, результатом реакции является образование спиртов. Атом галогена в галогеналкане замещается на гидроксогруппу.
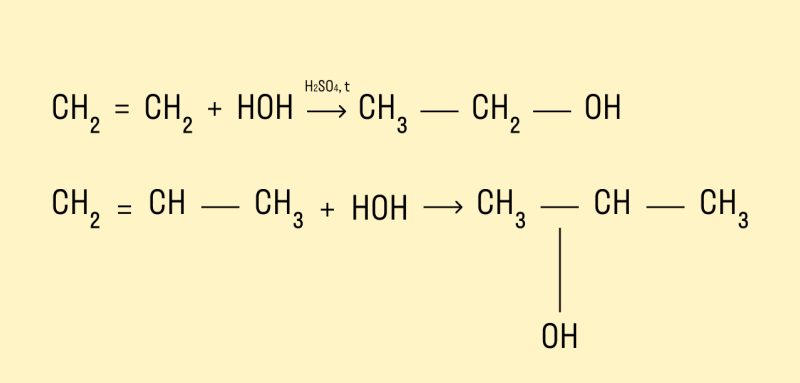
Гидратация алкенов
Присоединение молекул воды происходит в присутствии минеральных кислот и при нагревании.
Если в реакцию вступают несимметричные алкены, то процесс гидратации подчиняется правилу Марковникова. Атом водорода присоединяется к наиболее гидрированному атому углерода, а гидроксогруппа соединяется с соседним атомом углерода, наименее гидрированным.
Восстановление альдегидов и кетонов
Восстановление проводят каталитическим гидрированием карбонильной группы. Катализаторами могут быть никель, платина, палладий. Первичные спирты образуются из альдегидов, вторичные — из кетонов.
СН3—СНО + Н2 → CH3—CH2—OH
CH3—C(O)—CH3 + H2 → CH3—CH(OH)—CH3
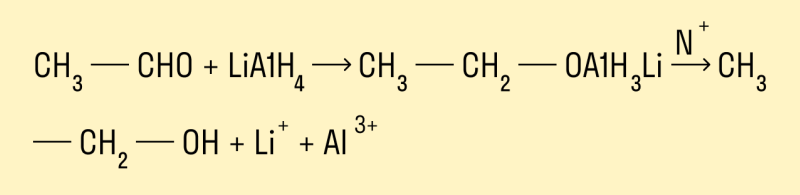
Альдегиды и кетоны можно восстанавливать, действуя на них разными восстановителями, например, комплексным алюмогидридом лития LiAlH4.
Реакция Канниццаро
Это окислительно-восстановительная реакция диспропорционирования альдегидов в первичные спирты и карбоновые кислоты под действием оснований.
2СH3—CHO + NaOH → CH3—CH2—OH + CH3—COONa
Гидролиз сложных эфиров
Процесс гидролиза заключается в том, что под действием воды происходит расщепление сложных эфиров. Гидролиз может протекать в кислой и щелочной среде. Гидролиз в щелочной среде является процессом необратимым, так как происходит омыление, т. е. образование солей карбоновых кислот.
Синтез Гриньяра
Синтез с использованием реактива Гриньяра. Реактивы Гриньяра — магнийорганические соединения, содержащие ковалентную связь C—Mg. Чаще всего их получают из органилгалогенидов вида R—X, где X = Cl, Br, I и магния в безводной среде.
- Первичные спирты получают из муравьиного альдегида.
- Уксусный альдегид и другие альдегиды дают вторичные спирты.
- Кетоны и сложные эфиры образуют третичные спирты.
Получение метанола из синтез-газа
Основной промышленный метод получения метанола состоит из двух этапов:
- Получение синтез-газа с помощью паровой, парокислородной или пароуглекислотной конверсии природного газа.
- Синтез метанола путем восстановления оксида и диоксида углерода водородом на катализаторе.
Этанол можно получить путем ферментативного брожения глюкозы (спиртовое брожение).
С6Н12О6 → 2C2H5OH + 2CO2
Реакция Вагнера
Окисление алкенов холодным раствором перманганатом калия в нейтральной среде (реакция Вагнера).
3CH2=CH2 + 2KMnO4 + 4H2O → HO—CH2—CH2—OH + 2MnO2 + 2KOH
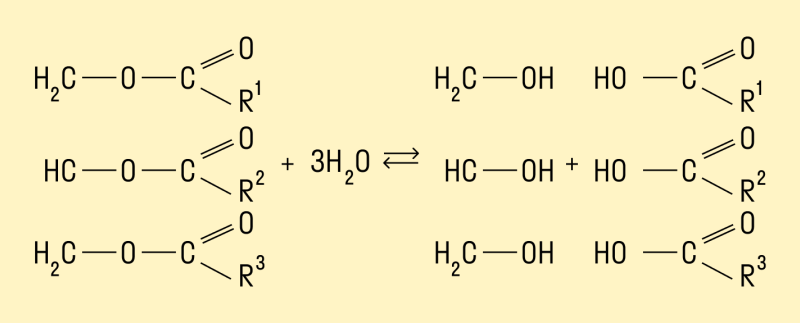
Гидролиз жиров
Многоатомные спирты можно получить путем гидролиза жиров. При взаимодействии кислот с жирами происходит образование глицерина и карбоновых кислот.
Какие последствия интоксикации?
Употребление изопропанола опасно не только симптомами отравления, но и последствиями. У человека есть большой риск развития:
- Заболеваний печени и почек (печень отравляется продуктами переработки вещества).
- Гастрита.
- Язвы желудка и ДПК.
- Параличей.
- Тяжелых дисфункций в работе нервной системы.
- Тяжелых расстройств гормональной системы.
Прогноз при отравлении заметно ухудшается, если больной выпил значительное количество спирта. Исход лечения будет зависеть от того, насколько квалифицированно и качественно проводилось лечение.
Видео: изопропанол (изопропиловый спирт).
Физические свойства изопропанола
Вещество в жидком состоянии имеет плотность 0,79 г/см3. Такая плотность ниже, чем у воды, поэтому изопропанол более летучий, чем вода. Он начинает кипеть при 83 градусах Цельсия. При концентрации более 2,5% в определенных условиях может взрываться. Самопроизвольное воспламенение происходит при нагреве до температуры выше 450 градусов Цельсия. Сочетание паров изопропилового спирта с воздухом способно образовывать взрывоопасную взвесь.
Спирт неплохо растворяется в ацетоне, бензоле. При добавлении в смесь воды и изопропанола поваренной соли он выделяется в отдельную фракцию.
Еще одним свойством изопропанола является постепенное увеличение вязкости при охлаждении. При значениях ниже – 70 °С имеет сиропообразную консистенцию.
Наиболее сильная линия поглощения молекул изопропанола приходится на ультрафиолетовую часть спектра (204 нм).
Почему для стерилизации используют 70% спирт, а не 100?
В то время как 70% раствор изопропилового спирта медленнее проникает в клеточную стенку и коагулирует весь белок клеточной стенки, и микроорганизм погибает. Таким образом, 70% раствор ИПС в воде более эффективен, чем 100% абсолютный спирт, и обладает большей дезинфицирующей способностью.
Как вы думаете, почему 100% спирт не используется для стерилизации или дезинфекции? 100% изопропиловый спирт мгновенно коагулирует белки, создавая белковый слой, который защищает другие белки от дальнейшей коагуляции. Благодаря этому микробы не погибают, а остаются в спящем состоянии.
Перекись водорода — это медицинский спирт?
Перекись водорода и медицинский спирт являются дезинфицирующими средствами и обычно используются для уборки дома.. Перекись водорода представляет собой соединение, образованное комбинацией кислорода и водорода, тогда как медицинский спирт является очень ядовитой формой этилового спирта или, проще говоря, спирта.
Можно ли использовать изопропиловый спирт на коже? Изопропиловый спирт убивает или предотвращает рост бактерий на коже. Изопропиловый спирт для местного применения (для нанесения на кожу) используется для предотвращения бактериальных инфекций кожи от незначительных порезов или царапин.. Изопропиловый спирт используется в медицинских учреждениях для предотвращения инфекций, которые могут быть вызваны проколами иглы.
Изопропиловый спирт – применение в быту, где продается и чем опасен
› Советы
Изопропиловый спирт представляет собой бесцветную жидкость с резким специфическим запахом. Другое название вещества, которое часто можно встретить – изопропанол, диметикарбинол, 2-пропанол, ИПС.
Широкое применение изопропилового спирта в различных отраслях обусловлено его химическими свойствами.
Свойства ИПС
- Смешивается с водой и ругими органическими растворителями;
- Растворяет почти все смолы и масла;
- Не вступает в химические реакции с растворами солей;
- Замерзает при температуре ниже -90 градусов.
ИПС является аналогом этилового и метилового спирта, при этом отличается более безопасным составом, доступностью и низкой ценой.
Он нашел свое применение в разных отраслях промышленности, косметологии и медицине, а также в быту.
в промышленности
Наибольшее распространение в отраслях промышленности изопропиловый спирт получил благодаря тому, что способен растворять большую часть масел и смол, при этом быстро испаряется с поверхности и повреждает ее. Помимо этого, он менее токсичен, чем другие растворители.
Наличие вышеперечисленных свойств позволяет использовать его в следующих отраслях промышленности:
- Мебельная и лакокрасочная. Здесь изопропиловый спирт применяется для того, чтобы растворять клей, краску и масла;
- В электронике. Им обезжиривают и осушают различные производимые детали и соединения;
- Фармацевтика. Служит в качестве исходного сырья для большого количества фармацевтических товаров;
- Химическая промышленность. Выступает в качестве промежуточного звена при получении других растворителей и является сырьем для промышленного производства ацетона;
- Лесохимическая – извлечение смолы из древесины;
- Полиграфии и типографии – помогает увеличивать яркость цвета при печати;
- Автохимия. Изопропиловый спирт применяется при производстве незамерзающей жидкости, антифриза;
- Бытовая химия. Добавляется во влажные салфетки очищающие средства.
Места продажи
Купить изопропиловый спирт достаточно сложно. Для этого можно обратиться напрямую к производителю, но в таком случае, возможна только оптовая закупка. В аптеке это вещество просто так купить не получится, для этого потребуется рецепт от врача. Для бытовых целей можно приобрести небольшое количество специализированных магазинах, занимающихся продаже химических реактивов.
Меры предосторожности
Как и любое химическое соединение, ИПС – опасное вещество, которое требует осторожного обращения. Использовать спирт необходимо в хорошо проветриваемом помещении, так как переизбыток его паров и попадание в организм могут привести к интоксикации. Хранить ИПС необходимо вдалеке от огня и попадания прямых солнечных лучшей, в местах, недоступных для детей
Хранить ИПС необходимо вдалеке от огня и попадания прямых солнечных лучшей, в местах, недоступных для детей.
https://youtube.com/watch?v=AV3aSQWuzkc
Спирт не обладает способностью впитываться в кожные покровы, но при регулярном взаимодействии может привести к химическому ожогу. Категорически запрещается допускать попадания веществ на слизистые оболочки.
Отравление изопропиловым спиртом: симптомы и первая помощь
Воздействие изопропилового спирта детально изучено специалистами. Результаты исследований указывают на то, что такое вещество действительно оставляет в организме человека следы, запуская необратимые процессы. В худшем случае при злоупотреблении такой жидкостью больной может впасть в кому или умереть.
Механизм интоксикации
Рассмотрим подробнее влияние изопропанола на организм. Отравление этим спиртом развивается в несколько этапов:
- Спирт всасывается в стенки желудка и проникает в кровоток.
- В печени обезвреживается около 80 — 90 % соединения.
- В малых количествах неизмененный спирт выходит из организма вместе с выдыхаемым воздухом и с мочой.
- Около 10 — 20 % изопропанола остается в кровотоке и превращается в ацетон.
- В крови резко возрастает уровень кетоновых тел. Ацетон поражает ткани почек, мозга и печени.
Токсические вещества самостоятельно выходят из организма только через 7 — 8 часов после приема спирта. В течение этого времени ацетон оказывает негативное воздействие на различные органы.
Чем изопропанол вреден для здоровья человека?
Изопропанол относится к группе спиртов, а значит, полностью сохраняет их свойства как положительные, так и отрицательные.
При сжигании ИПС в закрытом помещении у человека появятся симптомы отравления. От его горения образуется вода и углекислый газ, который в избытке опасен для здоровья. Температура вспышки изопропилового спирта — 82,5 °C.
Можно ли употреблять изопропиловый спирт? — нет, это равносильно распитию яда, пусть даже и с замедленным действием. Дело в том, что при поступлении в организм любое вещество преобразуется в печени, а фермент, который расщепляет изопропиловый спирт (алкогольдегидрогеназа) превращает его в ацетон. Всем известно, что последний не должен в норме присутствовать в тканях и органах человека.
В чём отличие изопропилового и этилового спирта? Изопропанол более токсичен, у него более сильное опьяняющее действие, а привыкание или наркотический эффект развивается быстрее. Употребление всего 50 мл изопропанола или интенсивное вдыхание его паров приведёт к развитию симптомов отравления.
Дети могут отравиться и меньшим количеством, чаще с признаками интоксикации в больницу поступают малыши до 6 лет.
Попав в организм человека, изопропиловый спирт может долго разлагаться от 2,5 до 8 часов. За это время вещество успевает повлиять негативно на все внутренние органы.
Небольшое количество пострадавших употребляют его в составе стеклоомывающих жидкостей. К этой категории обычно относятся БОМЖи и больные, страдающие заключительными стадиями алкогольной зависимости. По причине имеющейся в большинстве случаев алкогольной энцефалопатии подобные люди не могут адекватно оценить токсические свойства употребленного вещества.
Случайные или умышленные отравления изопропанолом в среде социально благополучных представителей общества практически не встречаются. В редких случаях интоксикация диагностируется у детей, не осознающих, что такое изопропиловый спирт и какую опасность он представляет для жизни.
Отравление изопропанолом происходит по следующей схеме:
- Всасывание спирта со слизистых оболочек желудка.
- Попадание в системный кровоток.
- Переработка 80%-90% отравляющего вещества в печени под воздействием фермента алкогольдегидрогеназы.
- Выделение небольшого количества неизмененного изопропанола через легкие и почки.
- Технический изопропанол частично остается в крови и расщепляется до ацетона.
- Развивается кетонемия, токсическое действие на печень, почки, мозг.
Период полувыведения изопропилового спирта в среднем составляет 7 часов. Он выводится с мочой, выдыхаемым воздухом, слюной, желудочным соком.
Попав в организм, независимо от способа, изопропанол оказывает тройное воздействие: опьяняющее, по типу алкоголя, токсическое, наркотическое. Опьянение наступает быстрее и более сильное, чем во время приема алкоголя: 10 мл выпитого вещества эквивалентно 100 мл чистого этанола.
Если количество выпитого достигает 40-50 мл у взрослого человека, возникает угроза здоровью, а доза около 300 мл может стать смертельной. Для детей это количество вдвое-втрое меньше, в зависимости от возраста.
Отравиться можно и парами вещества. Такое может быть, если вещество было разлито внутри закрытого помещения, и человек длительное время вдыхал пары ядовитого вещества. Пары изопропанола вызывают поражение глаз и дыхательных путей.
Изопропиловый спирт
Изопропиловый спирт используют в большинстве современных стеклоомывающих жидкостей. Водный раствор, содержащий 45 % об. изопропанола, замерзает при температуре −25 °C. При увеличении содержания объемной доли спирта в водном растворе температура замерзания такого раствора будет уменьшаться до определенных значений. Изопропиловый спирт имеет неприятный резкий запах, напоминающий запах ацетона, который трудно перебить даже концентрированными отдушками.
Изопропиловый спирт разрешен к использованию при производстве стеклоомывающих жидкостей.
Изопропиловый спирт отнесен к 3-му классу опасности (вещества умеренно опасные). Согласно Постановлению Главного государственного санитарного врача РФ от 28 января 2021 года № 2 “Об утверждении санитарных правил и норм СанПиН 1.2.3685-21 “Гигиенические нормативы и требования к обеспечению безопасности и (или) безвредности для человека факторов среды обитания” установлена предельно допустимая концентрация (ПДК) изопропанола в воздухе рабочей зоны: 50 мг/м3 (максимально разовая), 10 мг/м3 (среднесменная).
Технический изопропиловый спирт является легковоспламеняющейся жидкостью, пары которой образуют с воздухом взрывоопасные смеси. Изопропанол опасен при вдыхании и ядовит при приеме внутрь. Его пары вызывают раздражение слизистых оболочек, при контакте с кожей он может вызвать аллергическую реакцию
Важно обратить внимание на то, что в состав стеклоомывающих жидкостей входят водные растворы спиртов, массовая концентрация которых, как правило, составляет около 30 %
Как можно отравиться
Отравиться изопропилом можно случайно. Чаще всего люди выпивают взрывоопасную жидкость, спутав ее с водкой.
В группе риска по отравлению люди из неблагополучных категорий населения: алкоголики, лица с психическими расстройствами, бомжи, употребляющие раствор в составе стеклоомывателей для автомобилей.
Зафиксированы редкие случаи умышленного употребления вещества. Изредка отравляются жидкостью дети, которые выпивают раствор, не зная об опасности.
Как происходит отравление:
- Вначале соединение всасывается со слизистых поверхностей желудка.
- Затем проникает в систему кровообращения.
- Примерно 80% вещества перерабатывается в печени.
- Небольшой объем изопропанола выводится через дыхательные пути и почками.
- 10% спирта в чистом виде остается в кровеносной системе и преобразуется в ацетон.
- Развивается ацетонемия, которая отрицательно воздействует на печень, почечную систему и мозг.
В среднем соединение выводится за 7 часов.
Производство
В 1994 году 1,5 миллиона тонн изопропилового спирта было произведено в США, Европе и Японии. Он в основном производится путем объединения воды и пропена в реакции гидратации или путем гидрирования ацетона . Существует два пути процесса гидратации, и оба процесса требуют отделения изопропилового спирта от воды и других побочных продуктов путем дистилляции . Изопропиловый спирт и вода образуют азеотроп , и простая перегонка дает материал, который содержит 87,9% по массе изопропилового спирта и 12,1% по массе воды. Чистый ( безводный ) изопропиловый спирт производитсяазеотропная перегонка влажного изопропилового спирта с использованием диизопропилового эфира или циклогексана в качестве азеотропных агентов.
Непрямое увлажнение
Непрямая гидратация вступает в реакцию пропена с серной кислотой с образованием смеси сложных эфиров сульфатов. В этом процессе может использоваться пропен низкого качества, и он преобладает в США. Эти процессы дают в первую очередь изопропиловый спирт, а не 1-пропанол, потому что добавление воды или серной кислоты к пропену следует правилу Марковникова . Последующий гидролиз этих сложных эфиров водяным паром дает изопропиловый спирт перегонкой. Диизопропиловый эфир является важным побочным продуктом этого процесса; его возвращают в процесс и гидролизуют с получением желаемого продукта.
- СН 3 СН = СН 2 + Н 2 О(CH 3 ) 2 CHOH
Прямое увлажнение
Прямая гидратация вступает в реакцию с пропеном и водой в газовой или жидкой фазе при высоких давлениях в присутствии твердых или кислотных катализаторов на носителе . Для этого типа процесса обычно требуется пропилен более высокой чистоты (> 90%). Прямая гидратация чаще используется в Европе.
Гидрирование ацетона
Изопропиловый спирт может быть получен с помощью гидрирования из ацетона , однако этот подход предполагает дополнительный шаг по сравнению с описанными выше способами, так как ацетон сам обычно получает из пропена с помощью способа производства кумола . Это может оставаться экономичным в зависимости от стоимости продуктов. Известная проблема — образование МИБК и других продуктов самоконденсации. Никель Рене был одним из первых промышленных катализаторов, современные катализаторы часто поддерживаются биметаллические материалы. Это эффективный процесс и простой
Общее описание
Изопропиловый спирт — это прозрачная субстанция, характеризующаяся резким едким ароматом. Относится изопропанол к 3 классу опасности. Его используются для изготовления перекиси водорода и ацетона. Этот спиртовой состав также добавляется в косметику, парфюмерию и средства для дезинфекции и чистки поверхностей.
Изопропил очень огнеопасный элемент, поэтому пользоваться им нужно очень аккуратно и осторожно, соблюдая инструкцию. Вещество может раздражать слизистые органов дыхания и кожные покровы
При превышении концентрации оно может запросто стать причиной отравления.
Реакции
Изопропиловый спирт можно окислить до ацетона , который представляет собой соответствующий кетон . Этого можно достичь, используя окислители, такие как хромовая кислота , или дегидрированием изопропилового спирта над нагретым медным катализатором
- (CH 3 ) 2 CHOH → (CH 3 ) 2 CO + H 2
Изопропиловый спирт часто используется как источник как растворителя, так и гидрида в реакциях восстановления Меервейна-Понндорфа-Верли и других реакциях гидрирования с переносом . Изопропиловый спирт может быть преобразован в 2-бромпропан с использованием трибромида фосфора или дегидратирован в пропен путем нагревания с серной кислотой .
Как и большинство спиртов, изопропиловый спирт реагирует с активными металлами, такими как калий, с образованием алкоксидов, которые можно назвать изопропоксидами . Реакция с алюминием (инициированная следами ртути ) используется для приготовления катализатора изопропоксида алюминия .
В заключение, изопропиловый спирт — это прозрачная, бесцветная жидкость, которая является обычным растворителем и дезинфицирующим средством. Он состоит из трех атомов углерода, восьми атомов водорода и одного атома кислорода и легко воспламеняется. Изопропиловый спирт часто используется в качестве растворителя, дезинфицирующего средства и чистящей жидкости, а также содержится во многих бытовых товарах. Его получают путем реакции пропилена с серной кислотой, а затем добавляют воду. Несмотря на широкое применение, с изопропиловым спиртом следует обращаться осторожно, так как он легко воспламеняется и токсичен при попадании в организм.