Галоген — химические и физические свойства газа
Содержание
- 1 О галогенах
- 2 Строение атомов и степени окисления
- 3 Распространённость элементов и получение простых веществ
- 4 Физические свойства галогенов
- 5 Химические свойства галогенов
- 6 Особенности добычи и использования галогенов
- 7 Применение галогенов и их соединений
- 8 Галогенные соединения и их роль в организме человека
- 9 Видео
Элементы 17 группы таблицы Д.И. Менделеева – галогены. Классические неметаллы, в чистом виде в природе не встречающиеся. Галоген – это активный окислитель, он находится только в качестве соединений. За исключением отдельных неметаллов, с галогенами реагируют все обычные вещества.
О галогенах
Из галогенов лишь йод способен обладать признаками свойств, характеризующих металлы. Другие вещества (бром, хлор, астат и фтор) лишены даже косвенных признаков металлов. Когда в 1811 году И. Швейггер, немецкий химик, предложил так называть новое выделенное вещество – хлор, название не прижилось. С 1841 года галогенами стали называть всю группу «солеродов». Так переводится с греческого языка слово галогены.
Можно лучше понять, что такое галоген, если охарактеризовать каждый из элементов, входящих в этот ряд:
- Фтор (F) – содержится в солях горных пород. Преимущественно им насыщены криолит, шпат плавиковый и минералы флюорита;
- Хлор (Cl) – популярный из галогенов, в мире имеется в хлориде натрия, являющегося главным сырьём для хлористых соединений;
- Бром (Br) – элемент, встречающийся в морских водах и солёных водоёмах в качестве соли калия и натрия в сочетании с сульфатами хлора;
- Йод (I) – встречается повсеместно, больше всего йода в морской капусте и водорослях;
- Астат (At) – искусственное вещество в природе не встречается, получают в результате оседания частиц при облучении висмута или тория.
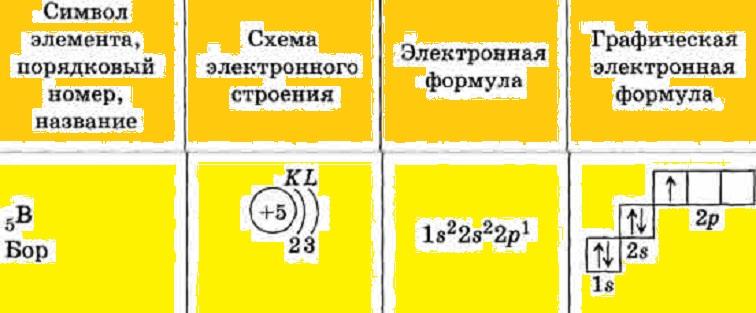
Строение атомов и степени окисления
Электронная формула наружной орбиты атомов солеродов – ns2np5. При расположении по порядку:
- F — 2s22p5;
- Cl — 3s23p5;
- Br — 4s24p5;
- I — 5s25p5;
- At — 6s26p5.
Атомы галогенов успешно добавляют к 7 своим электронам, имеющимся на крайней оболочке, один чужой недостающий. Потому при взаимодействии обнаруживают степень (-1) окисления. В союзах, где присутствуют элементы, имеющие электроотрицательность выше, только фтор не меняет степени (-1).
Остальные изменяют её на положительную степень: Cl (+1), Br (+3), I (+5), At (+7).
Распространённость элементов и получение простых веществ
Чем больше величина атомного радиуса, тем меньше наличие солеродов в теле планеты. Величина r – радиуса атома фтора, по сравнению с радиусом атома иода, говорит о том, что фтор более распространён, нежели йод. Астата в коре планеты всего лишь граммы.
Промышленность производит галоиды (устаревшее название) в больших объёмах. При этом по количеству изготовленной продукции лидирует хлор.
Простые вещества получают при помощи галогенидов, окисляя их. Для этого используется электролитическое окисление. Причём из-за того, что положительные потенциалы у фтора и хлора достаточно высокие, приходится применять сильные окислители.
Электролиз NaCl с применением анодов из графита позволяет добывать хлор. Катоды при этом могут быть:
- железные;
- жидкие ртутные;
- стальные.
Уравнение, описывающее эту реакцию, имеет вид:
2Cl- —› Cl2 (г.) + 2е-.
Выполняя химическое окисление бромида-иона из морской воды, получают бром.
Так же добывают и йод, используя насыщенные им рассолы. Оба процесса проводят, применяя хлор в виде окислителя. Воздушным потоком, проходящим через раствор, удаляются I2 и Br2.
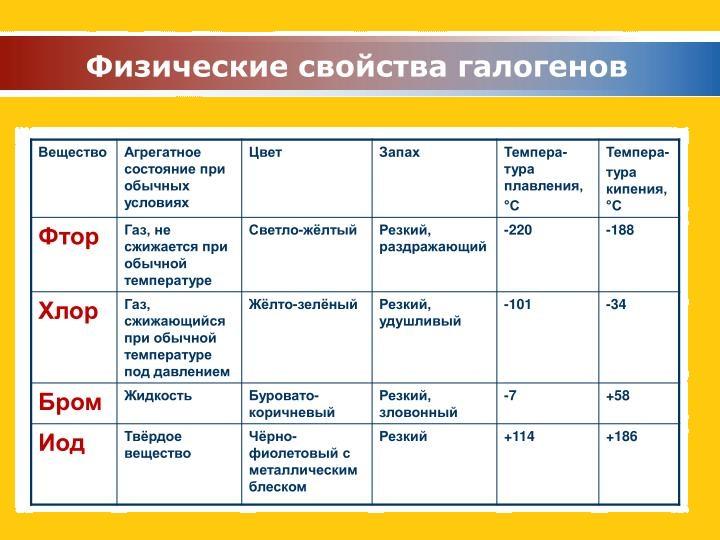
Физические свойства галогенов
Это характеристики, описывающие цвет, запах, температуры изменения свойств, а также агрегатное пребывание в нормальных условиях.
Химические свойства галогенов
Способность вступать в реакцию с разными веществами под воздействием сторонних факторов индивидуальна для каждого из рассматриваемых элементов.
При вступлении галогенов в связь с медью (малоактивный металл) получаются галогениды с формулой:
CuHal2, где Hal2 – солероды Br, Cl, F.
Когда галогениды вступают в реакцию с галогенами, то тот солерод, который активнее, вытесняет малоактивный из его же раствора. Хлор, являясь окислителем, вступает во взаимодействие в смесях солей йода и брома. Бром не реагирует на хлориды, но может из иодидов выдавить йод.
При воздействии на органические соединения при хлорировании воды или йодировании соли происходит галогенирование. При этом атом галогена вводится в соединение. Галогенирование может осуществляться замещением, расщеплением или присоединением атома солерода к атомной структуре органических соединений.
Интересно. Йод, имея низкие окислительные способности, не выдавливает из солей галогены. С фтором реакции водных сульфитов вообще не получаются, он вступает в содействие с Н2О.
Особенности добычи и использования галогенов
Приём электролизного окисления с участием окислителей применяется при добывании галогенов, исходя из того, что в натуральных условиях они – анионы. Например, гидролиз смеси поваренной соли необходим для выработки хлора. В основном, сначала добываются галогениды, из них электрохимическим путём изымаются солероды.
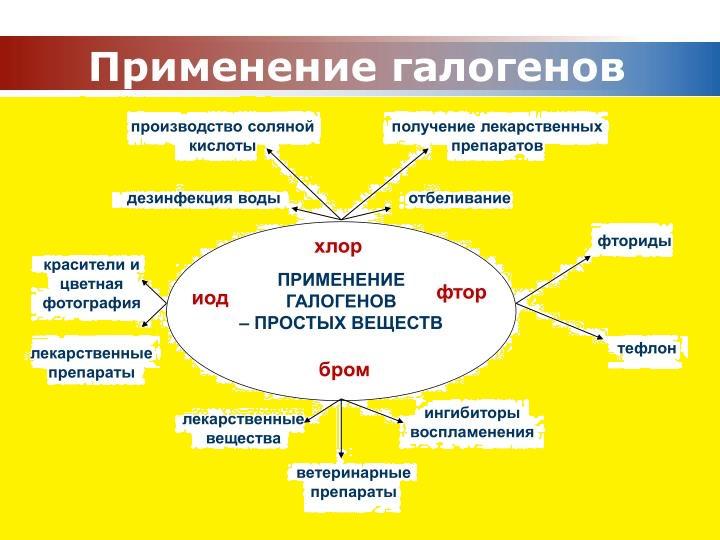
Применение галогенов и их соединений
Использование солеродов находит широкое применение в жизни человека. Быт, медицина, химическая промышленность, военное производство – далеко не все области использования солеродов.
По каждому элементу можно рассмотреть следующие моменты:
- F – значимая часть состава фторополимеров, имеющих высокую химическую, коррозионную и термическую стойкости. Фторсодержащие хлорфторуглероды раньше использовались в хладагентах и в аэрозолях.
- Cl – в натуральном виде газ жёлто-зелёного цвета. Хлор употребляется для обеззараживания скважин, воды для питья и искусственных водоёмов. Наиболее частое применение хлора в быту – отбеливание вещей и очищение загрязнённых поверхностей сантехники. Соляная (муриевая) кислота также содержит хлор.
- Br – негорючее вещество, применяется для тушения огня в огнетушителях. Применим бром и в медицине, в качестве успокоительных препаратов и мегалитических средств. В военных целях входит в состав химии отравляющих веществ.
- I – применяется в виде антисептика, является необходимым элементом в организме человека для работы щитовидной железы.
- At – применения не находит ввиду своей сильной радиоактивности.
Добавленный в баллон лампы накаливания газ галоген позволяет повысить температуру встраиваемой нити и качество отдачи света. Пары брома или йода, закачанные в колбу, послужили созданию галогенных ламп и светильников.
Галогеновый свет используется в лампах автомобильных фар, причём конструкция позволяет выполнять установку, как галогенных ламп накаливания в фару, так и обычных. В соревнованиях светодиодного источника в фаре или галогенового пока лидирует последний.
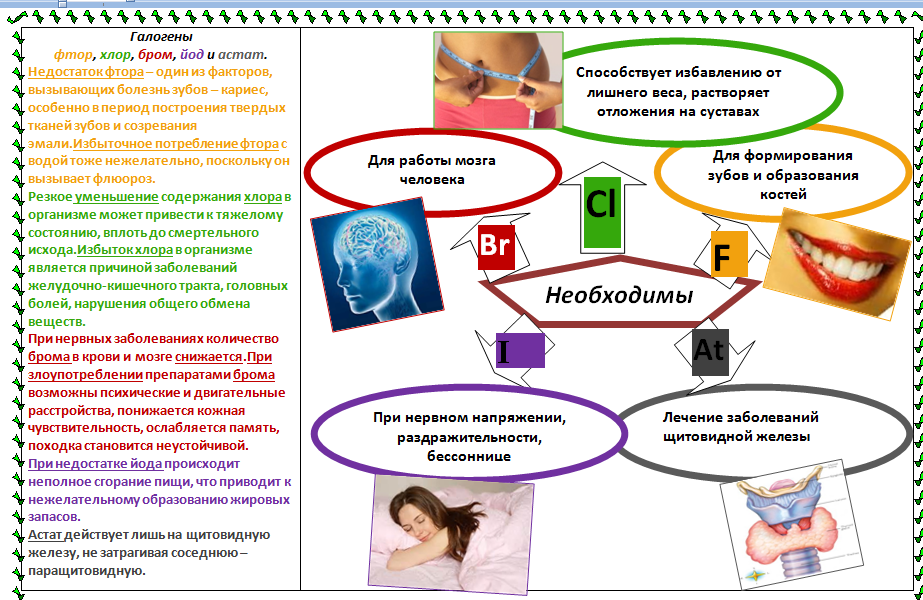
Галогенные соединения и их роль в организме человека
В человеческом организме в разных процентных содержаниях присутствуют соединения солеродов. Превышение концентраций, как и их уменьшение, существенно влияет на состояние организма.
Токсичность галогенов
Галогены в опасной концентрации и соединениях действуют на человека следующим образом:
- Хлор имеет 2 класс опасности. Концентрация в атмосфере от 1*10-4% уже вызывает раздражение слизистой, доза 0,01% приводит к острому отравлению и остановке дыхания. Это сильный канцероген, вызывающий туберкулёз и способствующий образованию злокачественных опухолей;
- Фтор в соединении фторида натрия – приводит к смерти, попадая внутрь через органы дыхания или пищеварения. Смертельная концентрация – 4-9 г. Первичные симптомы – слюнотечение, рвотные позывы. Вторичные признаки отравления – поражения нервной и сердечно-сосудистой систем.
- Бром вызывает спазмы и удушье при дыхании уже при концентрации 1*10-3 в объёме воздуха. Токсичная доза – 3 г., смертельная – от 34 г., при попадании внутрь человека.
- Йод, при случайном попадании в организм в количестве 3 г. и более, поражает почки и сердечно-сосудистую систему, блокирует рецепторы щитовидной железы.
Применение галогенов и галогенидов в промышленности и в быту приносит больше пользы, чем вреда. Знание допустимых значений концентрации и правил пользования продуктами, в которых применяются солероды, позволяет пользоваться только их положительными качествами.